Como ocurre con muchos descubrimientos interesantísimos, el equipo de Hubert Lam estaba investigando otro asunto cuando se produjo el hallazgo. En concreto el grupo estaba intentando delimitar el efecto que sobre la virulencia del cólera tiene la forma de la bacteria que lo produce, Vibrio cholerae. Los investigadores estaban trabajando con células en las que se habían mutado las proteínas que controlan la forma celular. Los investigadores se dieron cuenta que los enantiómeros dextrógiros, no así los levógiros, de cuatro aminoácidos eran los que estimulaban la transición de la forma bacteriana de barra a esfera.
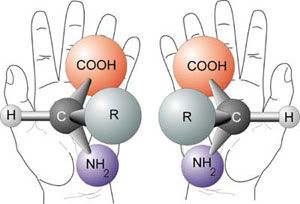
Conforme las células mutadas de V. cholerae pasaban de un crecimiento exponencial cuando eran barras a un estado estacionario cuando eran esferas, los investigadores pudieron comprobar que los L-aminoácidos se convertían en D-aminoácidos por la acción de unas enzimas llamadas racemasas, que tienen el efecto de alterar la estructura de la molécula alrededor del carbono asimétrico.
Para determinar en qué parte de la pared celular estaba actuando esta repentina acumulación de D-aminoácidos, los investigadores compararon células normales con otras mutadas en las que no se expresaban las racemasas (y no tenían por tanto una cantidad significativa de D-aminoácidos). Encontraron que en estas células un polímero elástico, la mureína (peptidoglicano), componente estructural principal de las paredes bacterianas, era más grueso pero más débil estructuralmente, prueba de que los D-aminoácidos tienen la capacidad de alterar la composición, cantidad y fuerza de la mureína.
El grupo comprobó entonces si estos resultados eran extrapolables a otras bacterias. Para ello eligieron
A la vista de los resultados, los autores lanzan la hipótesis de que las moléculas de derechas serían capaces de disminuir la actividad metabólica de cualquier célula bacteriana cuando los recursos se vuelven escasos o las condiciones ambientales adversas.
Referencia:
Lam, H., Oh, D., Cava, F., Takacs, C., Clardy, J., de Pedro, M., & Waldor, M. (2009). D-Amino Acids Govern Stationary Phase Cell Wall Remodeling in Bacteria Science, 325 (5947), 1552-1555 DOI: 10.1126/science.1178123
2 comentarios:
Muy divertido el título del post, "aminoácidos de derechas" je.
Aparte de pensar que el contenido del artículo es interesante (como todos los que nos traes), me he acordado de que cuando estudiaba bioquímica pensaba que podría haber un universo paralelo en el que toda la vida se basar en aminoácidos D. Técnicamente, a nivel molecular, sería factible un universo que fuese la imagen especular de este, creo. ¿En qué momento la evolución se "decantó por los aminoácidos "de izquierdas" y no por los "de derechas" para construir proteínas? Pues ni idea, pero son de esascosas que me hace gracia pensar.
Saludos
Gracias por el comentario, cope.
Lo de llamar de esa manera a los enantiómeros era cosa de una profesora mía de orgánica (no diré cual), izquierdosilla ella.
Respecto a la evolución, y puestos a especular, pensemos que cada organismo, en cada especiación replica del que procede casi toda su estructura molecular. A nivel de evolución química pudo pasar lo mismo: si la primera molécula que funcionó era levógira todo lo que la siguió serían variaciones sobre un mismo tema. Se me ocurre que esa primera molécula levógira tuvo que reunir dos características fundamentales: en primer lugar su éxito reproductor tuvo que basarse en una especificidad espacial alta, como es obvio, y segundo, el éxito reproductor tuvo que ser EL éxito reproductor por antonomasia. Estaríamos hablando de un estadio anterior al ARN, pero no demasiado alejado. Unos proto-ARN que no consiguen replicarse por impedimentos estéricos y que de buenas a primeras entra una molécula levógira que sí lo permite.
Es para darle unas vueltas al caldo (pun intended).
Un cordial saludo.
Publicar un comentario