Mientras que la mayoría de las teorías del envejecimiento hacen hincapié en los efectos del estrés, la radiación, la oxidación o la ingesta calórica como los factores principales que controlan la duración de la vida debido a que dañan el ADN, una nueva teoría afirma que el factor determinante viene incorporado al ADN desde el origen. Los autores de
La edad avanzada sigue siendo el principal factor de riesgo para muchas enfermedades graves: cardiovasculares, derrames cerebrales y cáncer. Los mecanismos por los que la edad avanzada predispone a la enfermedad están comenzando a comprenderse debido, en parte, a las manipulaciones ambientales y genéticas de organismos modelo.
Las datos sugieren que el daño al ADN podría ser la parte final común a varios de los mecanismos de envejecimiento propuestos. Esta nueva teoría supone que hay un mecanismo adicional que implica la existencia de una inestabilidad genética inherente al propio ADN.
Los LINE (Long Interspersed Nuclear Elements, elementos nucleares dispersos largos), constituyen el 20% del genoma humano. Son, ahora lo explicamos, retrotransposones no-LTR (Long Terminal Repeat). Un retrotransposón es un transposón, una secuencia de ADN que puede moverse autosuficientemente a diferentes partes del genoma de la célula, que emplea ARN como intermediario en este desplazamiento. Los LTR son secuencias de nucleótidos que se encuentran en los extremos de elementos retrovirales que están integrados en el genoma de la célula. Por tanto, un LINE es una secuencia de ADN que se puede mover a distintos sitios del genoma pero que no es parte de los extremos de un retrovirus integrado en el genoma.
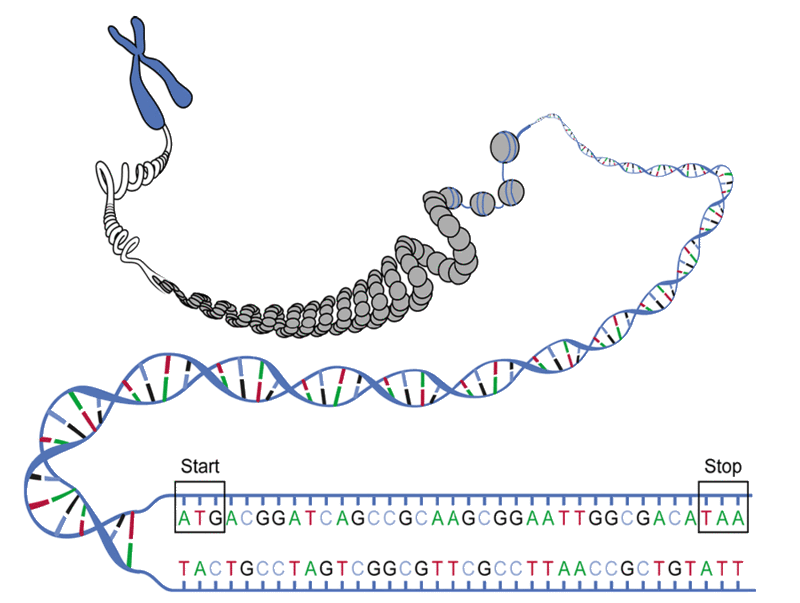
Pues bien, la familia de mayor importancia cuantitativa es LINE-1 o L1 que es una secuencia de 6 kilobases repetida unas 800.000 veces de modo disperso por todo el genoma. Dos de los productos de L1 son las proteínas ORF1p y ORF2p. Un ORF (Open Reading Frame), un marco abierto de lectura, en la imagen, es cada una de las secuencias de ADN comprendida entre un codón de inicio(Start) de la traducción y un codón de terminación (Stop). Estas proteínas son capaces de unirse al ARN y tienen una actividad que permite la retrotransposición. Aunque son principalmente activas sólo durante la embriogénesis, estas transcripciones de L1 se detectan en las células somáticas adultas en ciertas condiciones.
Lo que los autores plantean es que estos productos de la L1 funcionarían como un “reloj endógeno”, erosionando lentamente la integridad del genoma compitiendo con el mecanismo que vuelve a unir las dos hebras del ADN después de la copia. Así, si bien las transcripciones de la L1 son un mecanismo aceptado de variación genética (un motor de la evolución), se propone que la longevidad se ve negativamente afectada por la actividad somática de la propia L1. Es decir, el mecanismo que ha permitido evolucionar a los humanos sería el mismo que nos hace envejecer.
Referencia:
No hay comentarios:
Publicar un comentario